1.幹細胞と再生医療の現状
幹細胞は組織に応じた細胞に分化できる能力と、自らを複製する能力を有しています。幹細胞には、胚性幹細胞(ES細胞)、人工多能性幹細胞(iPS細胞)、体性幹細胞(成体幹細胞、組織幹細胞)などが知られており、再生医療等に活用されています。体性幹細胞である骨髄幹細胞は1960年代に発見され1)、現在、急性移植片対宿主病、脊髄損傷の治療薬として厚生労働省より承認を得ています。また、第二種再生医療等として国に提供計画が届けられ、脳梗塞の研究などが進められています2)。
ES細胞は1981年に英国の生物科学者マーティン・エバンス氏らが、マウスの胚盤胞の内側にある細胞を取出し、それを試験管の中で培養する条件を突き止めました3)。1998年に米国のジェームズ・トムソン(iPS細胞の作製を中山教授と同日に発表)氏がヒトのES細胞を作製することに成功しました4)。国内ではES細胞から作製した肝細胞を生まれつき重い肝臓病のある乳幼児に移植する医師主導の臨床試験が進められています。
また体性幹細胞である脂肪幹細胞は、2001年に脂肪組織中の間葉系幹細胞として発見されました5)。現在、肝硬変を対象とした他家脂肪組織由来幹細胞製剤の臨床試験が進められています。脂肪幹細胞を用いた研究および治療の進展はめざましく、第二種再生医療等の治療で多くの医療機関で用いられています2)。iPS細胞は、京都大学の山中伸弥教授によって、2006年にその作製が発表され6)、これまでも再生医療トピックスでご紹介しましたが、加齢黄斑変性、パーキンソン病、目の角膜の病気(角膜上皮幹細胞疲弊症)、重症心不全でそれぞれ移植が実施されています。
そして、2010年には東北大学の出澤教授によって新たな幹細胞が発見され、Muse細胞(Multi-lineage-differentiating Stress Enduring Cell)と名付けられました7),8)。
2.Muse細胞の概要9)
人の皮膚や骨髄などの中に、いろいろな組織や臓器に成長する能力を持つ新たな「多能性幹細胞」が存在することが、東北大大学院医学系研究科出澤教授らの研究グループによって明らかにされました。当該研究グループは、皮膚由来のヒト線維芽細胞や骨髄由来の骨髄間葉系細胞に長時間、低酸素や栄養がないなどのストレス条件を与えて細胞を濃縮し、これを浮遊培養したところ、人のES細胞とよく似た細胞の塊が形成されました。最初は時間と共に増殖しますが、10~14日程度で成長は停止し、無限に増えることはないとのことです。特別な処理を加えると、5代先まで自己複製できることが確認されています。ゼラチンで培養しますと、神経や平滑筋、肝臓などへ分化できることも確認されています。
Muse細胞は多能性幹細胞マーカーSSEA-3を指標に同定が可能であり、多様な細胞に分化する能力を有するとされています。傷害を受けた臓器から出されるシグナル(S1P:sphingosine-1-phosphate)を感知することで血液中のMuse細胞は傷害部位に集積し、組織を構成する複数の細胞種に分化することで傷害組織を健常組織に置き換えて修復することが報告されています。
このため、iPS細胞のように治療対象である臓器の心筋細胞、あるいは神経細胞などに事前に体外で分化誘導や増殖させる必要はなく、分化した細胞を外科的治療法で移植する必要はありません。また、Muse細胞は免疫抑制作用も有しているため、他人の細胞移植(他家移植)を行っても免疫拒絶反応のリスクを抑えることができると考えられています。Muse細胞による再生医療は、点滴による治療の可能性があります。この点滴での再生医療が可能となれば、特別の施設を有しない病院での治療も実現され、Muse細胞による治療効果の恩恵を受けることができるでしょう。
現在、国の承認を受けて三菱ケミカルホールディングス傘下の(株)生命科学インスティテュートが2018年1月から他家Muse細胞による急性期心筋梗塞への治験が、同年9月からは脳梗塞患者を対象とした治験が開始されています。現在、動物実験の段階ですが、脳梗塞モデル動物において神経機能の回復や慢性肝障害モデル動物での著しい肝機能の回復などが報告されています。細胞治療が他家細胞の点滴投与によって実現できれば、現在、国に届出された提供計画に基づく治療が進められている脂肪幹細胞などと相まって再生医療は大きく進むことが期待されます。
3.Muse細胞を用いた再生医療の研究開発動向
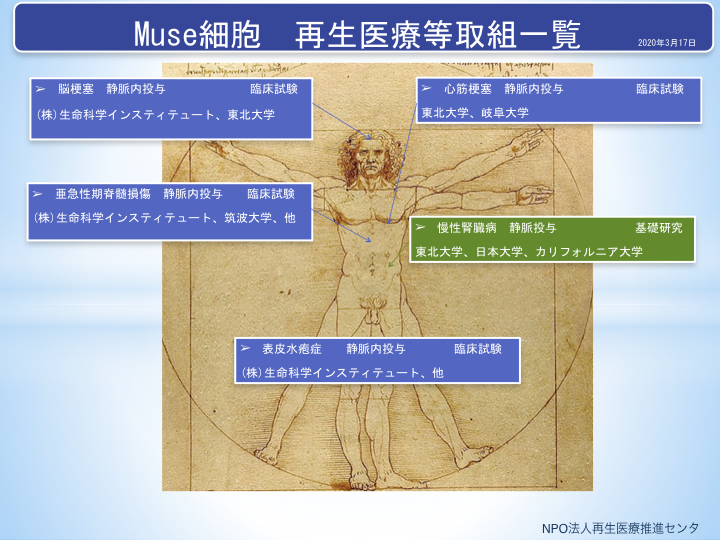
3.1 心筋梗塞 静脈内投与 臨床試験
Muse細胞を使って、心筋梗塞を起こしたウサギの心臓の機能を改善させることに成功したと、岐阜大学と東北大学のグループが発表し、現在、企業が中心となって臨床試験が進められています10),11)。岐阜大学と東北大学の研究グループは2018年3月6日、記者会見を開き、体のさまざまな組織の細胞に変化する能力があるとされているMuse細胞を、急性の心筋梗塞を起こしたウサギの血液中におよそ30万個投与したところ、2週間ほどで心臓の機能が改善したと発表しました。同グループによりますと、従来の骨髄由来幹細胞を用いた心筋梗塞治療の臨床研究では,心機能改善の十分な効果が得られていませんが、ウサギ心筋梗塞モデルで、多能性幹細胞のMuse細胞を静注したところ、S1P-S1PR2 axisを介して梗塞部位にMuse細胞が高率に生着し、作業心筋に分化し、paracrine効果も加わり,2週、2カ月,6カ月後に、劇的な梗塞サイズ縮小、心機能改善、左室リモデリング抑制が得られ、その効果は従来の骨髄由来幹細胞(MSC)よりも大きかったため,今後の臨床応用での有効性が期待されるとしています12)。
3.2 脳梗塞 静脈内投与 臨床試験
(株)生命科学インスティテュートは、脳梗塞患者さんを対象としたMuse 細胞製品(CL2020)の探索的臨床試験を東北大学病院にて2018年9月中旬から開始することを発表しました13)。脳梗塞を含む脳血管障害(脳卒中)は日本における入院原因の第2位であり、さらに要介護となる原因の第1位(介護保険で、介護が必要となった原因の2割弱)とされています。
これまでに実施した脳梗塞モデルを用いた動物試験では、CL2020の静脈内投与により、運動機能障害の改善効果を示すことが確認されたそうです。Muse細胞製品「CL2020」としては、前記の2018年1月に開始した急性心筋梗塞に次ぐ、第二の対象疾患の探索的臨床試験となります。CL2020は、傷害を受けた神経回路を修復することで運動機能障害を改善する可能性があり、脳梗塞治療の新たな選択肢になり得るとしています。Muse細胞は生体に存在する自然の多能性幹細胞であり、腫瘍性を持たず安全性が高く、Muse細胞は血管内や局所に投与するだけで傷害部位を認識して生着、組織に応じた細胞に自発的に分化して修復します。目的とする細胞への事前の誘導操作を必要とせず、投与するだけで再生治療の可能があるとしています14),15)。
3.3 亜急性期脊髄損傷 静脈注射 臨床試験
(株)生命科学インスティテュートは、脊髄損傷を対象疾患として、Muse細胞製品「CL2020」の臨床試験を国内で開始すると発表しました(2019年7月9日)16)。現在の脊髄損傷の治療では、運動麻痺および感覚麻痺痺の十分な改善が得られず、長期間にわたって患者さん、並びにご家族にとりましても経済的、社会的、精神的な負担となります。我が国では、年間4〜5千人が受傷し、総患者数は10〜20 万人と推計されています。このような観点から、有効な新規の治療法が期待されています。
Muse細胞は末梢血や骨髄、および各臓器の結合組織中に分布している内因性の修復幹細胞で、遺伝子の導入や事前に分化誘導したり、外科手術で細胞を移植したりする必要もなく、そのまま静脈内に投与するだけで損傷部位に集積し、そこに生着して組織を修復するという特徴を有しています17)。同社によりますと、脊髄損傷モデルラットにCL2020を急性期から亜急性期に1回または2回静脈内投与した結果、後肢運動機能の改善効果が認められ、歩行可能となり、投与時期や投与回数が異なっていても、運動機能の改善効果が認められたとのことです。ラットの体内の脊髄が傷ついた部分からはシグナル(S1P)が出ていて、投与されたMuse細胞が、そのシグナルをキャッチして自ら傷ついた部分に移動し、新しい神経細胞になって修復したと考えられるとしています。そこで、臨床において単回投与による有効性と安全性を検討するに至りました。
臨床試験の概要ですが、対象疾患としては、受傷から2週間程度の亜急性期患者(16歳以上75歳未満)さんに対し、CL2020を単回静脈投与による有効性と安全性を検討します。筑波大学附属病院ほか10施設で行うことを予定し、非盲検、非対照で行い、目標の症例数は10症例としています。亜急性期を対象にした理由は、急性期の炎症が収束し、血管新生・組織修復反応が盛んに起こるためとしています。早ければ2020年度にも承認申請をしたい考えとのことです。
なお、2020年1月9日、Muse細胞製品の亜急性期脊髄損傷患者を対象とした臨床試験での被験者募集について発表されています18)。
3.4 表皮水疱症 静脈投与 臨床試験
生命科学インスティテュートは、表皮水疱症の治療に向け、Muse細胞を用いた「CL2020」の探索的臨床試験を開始することを発表しました(2018年12月20日)19)。表皮水疱症とは表皮-基底膜-真皮の接着を担っている接着構造分子が生まれつき少ないか、消失しているために、日常生活のわずかな刺激で水疱、潰瘍が生じてしまう病気です。国の指定難病に登録されており、国内に500~1000人の患者さんがおられます。現状では有効な治療法はありません。臨床試験は、難治性潰瘍を有する12歳以上の患者さんです。症例は5例で、複数の医療機関で実施し、安全性、有効性を検討するとしています。
3.5 慢性腎臓病 静脈投与 基礎研究
出澤教授の研究グループは、日本大学医学部およびカリフォルニア大学ロサンゼルス校の研究グループと共同で、ヒトMuse細胞を慢性腎臓病モデルマウスに静脈投与すると、腎組織が修復され腎機能が回復することを明らかにしました20)。ヒト細胞を拒絶しない免疫不全マウスにおいて薬剤投与によって慢性腎臓病モデルを作成し、ヒト骨髄由来のMuse細胞を静脈投与したところ、傷害を受けた腎臓の糸球体に選択的に生着し、自発的に糸球体を構成する細胞として分化したそうです。
糸球体構成細胞に分化したMuse細胞は投与後7週においても腎臓内で生存し、腎機能が改善されたとのことです。一方、免疫機能が正常なマウスモデルで免疫抑制剤を投与せずに同様の実験を行ったところ、ヒトMuse細胞は5週までは分化・生存し、顕著な腎機能の回復を示したが、7週後になると排除され、腎機能も悪化したことから、Muse細胞が糸球体構成細胞として生着していることが腎機能回復に直接寄与していることが示されたとしています。これらの結果から、Muse細胞の点滴投与で慢性腎臓病を修復再生できること、またドナーのMuse細胞が長期間にわたってレシピエントの体内に残り、回復効果をもたらす可能性が示されました。
(参考資料)
(NPO法人再生医療推進センター 守屋好文)