
わが国で慢性腎臓病などの疾患により、透析治療を受けている患者数は33万人とされており、増加傾向にあります。根本的治療には生体腎移植が最も有効とされていますが、腎臓移植希望登録数の約12,500件に対して、腎臓移植例は約1,750件と報告(日本移植学会2019年1月公表)されています。こうした状況を克服するためにiPS細胞などから腎臓を作り出す取組がなされておりますが、現状では、立体的、かつ移植に適したサイズの腎臓を生み出すまでには至っておりません。
ここでは、iPS細胞を使用した3つの基礎研究についてご紹介致します。最初はヒトiPS細胞由来の腎前駆細胞を用いた細胞療法の基礎研究です。次に、先天性腎臓病患者さん由来のヒトiPS細胞から腎臓組織を誘導することによって、病態解明や治療に関する基礎研究です。最後は、iPS細胞を用いた「胎生臓器ニッチ法」による腎臓再生医療の基礎研究についてです。
(1) 慢性腎臓病 ヒトiPS細胞 細胞療法 マウス 基礎研究
◎京都大学 iPS細胞研究所
同研究所の長船教授らの研究グループは、ヒトiPS細胞から誘導した腎前駆細胞注1)を効率よく単離できる表面抗原マーカー注2)の組み合わせを見出しました1-2)。その表面抗原マーカーを用いて単離した腎前駆細胞を急性腎傷害モデルマウス注3)に移植し、腎機能悪化および線維化注4)を抑制する治療効果を確認しました。
主な研究成果は、次の通りです。
① ヒトiPS細胞由来の腎前駆細胞を効率よく単離できる表面抗原マーカーを同定
研究グループは、ヒトiPS細胞から誘導した腎前駆細胞を用いて242種類の表面抗原マーカーのスクリーニングを行、その結果、ある表面抗原マーカーの組み合わせ(CD9(-)CD140a(+)CD140b(+)CD271(+))が、治療効果を持つOSR1(+)SIX2(+)の腎前駆細胞と一致率が高いことを見出しました。
② 表面抗原マーカーを用いて単離した腎前駆細胞の機能の評価
表面抗原マーカーを用いた単離により、腎前駆細胞マーカーであるOSR1、SIX2、HOXD11を発現する細胞を濃縮できることが免疫染色で確認しました。CITED1、CDH11(Cadherin 11)、ITGA8(Integrin alpha 8)、HOXA11などの他の腎前駆細胞マーカーの発現上昇も確認しました。さらに、単離分取した細胞を細胞塊にして誘導すると尿細管様注4)の構造が形成されました。
③ 急性腎傷害モデルマウスにおいて細胞療法の治療効果を確認
表面抗原マーカーにより単離した腎前駆細胞を急性腎傷害モデルマウスに移植すると、移植群において有意に腎機能の悪化を抑制しました。また、移植後12日目の組織評価では、移植群において有意にホスト腎臓の線維化を抑制していることが確認されました。
研究成果は、ヒトiPS細胞由来の腎前駆細胞を用いた細胞療法の臨床応用や、腎疾患モデル作製への貢献が期待されます。
(2)小児腎臓病 ヒトiPS細胞 マウス 病態解明/治療 基礎研究
◎熊本大学、順天堂大学、琉球大学、広島大学
熊本大学西中村隆一教授らの研究グループは、先天性腎臓病患者さん由来のヒトiPS細胞から腎臓組織を誘導することによって、病態を再現することに成功したと発表しました(2018年8月27日)3)。腎臓は血液中の老廃物などをろ過して尿として排出します。糸球体注5)のポドサイト注6)に存在するろ過膜により、血液中の蛋白質は尿中には漏れません。ネフリン注7)という物質がその主な構成要素です。ネフリンに遺伝子変異があると、血液中の蛋白質が尿に大量に漏れ、先天性のネフローゼ症候群注8)になります。根治的な治療は困難で、ろ過膜を人工的に再現する技術が確立されていないために、研究進展の壁となっていました。
西中村隆一教授らの研究グループは2014年に、ヒトiPS細胞から腎臓組織を試験管内で誘導することに成功し3)、その後2016年には、iPS細胞から誘導した糸球体ポドサイトがネフリンを発現していること、誘導の途中にマウスに移植するとポドサイトがより成熟することを明らかにしました。今回、同教授のチームのメンバーらが、これらの方法を先天性腎臓病の患者さん由来のiPS細胞に応用しました。
主な研究成果は次の通りです。
①腎臓のろ過膜を構成するネフリンに変異をもつ先天性ネフローゼ症候群の患者さんの皮膚からiPS細胞を樹立しました。
②患者さん由来のiPS細胞から誘導した腎臓組織において、ネフリンの細胞表面への移行とろ過膜の形成に異常がみられたことにより、この先天性腎臓病の初期病態をiPS細胞で再現することに成功しました。
③これらの異常は、ネフリンの変異を修復することによって正常化し、この変異が病気を起こす原因であり、それを元に戻すと治療できる可能性を示めしました。 同研究は、患者さん由来のiPS細胞を使って糸球体性腎疾患の病態を再現した初めての例であり、病因の解明と創薬開発への貢献が期待されます。
(3)慢性腎臓病 ヒトiPS細胞 胎生臓器ニッチ法 基礎研究
◎大日本住友製薬(株)、明治大学、東京慈恵会医科大学
大日本住友製薬(株)らはバイオス(胎生臓器ニッチ法の技術を有する東京慈恵医大発バイオベンチャー)、ポル・メド・テック(ヒト腎臓再生医療用遺伝子改変ブタの技術を有する明大発バイオベンチャー)と共同で、iPS細胞を用いた「胎生臓器ニッチ法」による腎臓再生医療の研究開発を進め、2020年代での事業化の実現を目標として、共同研究・開発などの取組みを開始したと発表しました(2019年4月5日) 5-6)。 「胎生臓器ニッチ法」は、東京慈恵医科大学腎臓・高血圧内科学の横尾隆教授らの研究に基づく手法です。動物の発生段階である胎仔の中で臓器が発生する場所(臓器ニッチ)に、別の動物から目的とする臓器の前段階となる前駆細胞を注入し、臓器に分化誘導する方法です。発表された腎臓再生には、ヒトiPS細胞から分化誘導したネフロン前駆細胞注9)を、明治大学バイオリソース研究国際インスティテュート長嶋比呂志教授らの研究に基づく成果である「ヒト腎臓再生医療用遺伝子改変ブタ」の胎仔から採取した腎原基注10)に注入し、その後、腎原基を患者さんに移植することによって、臓器ニッチを利用した機能的腎臓の再生を目指す目論見です。
産学連携チームは、次の手順で腎臓再生医療に取り組む計画です。
① ヒトiPS細胞からネフロン前駆細胞へ分化誘導
② 遺伝子改変ブタ胎仔の膀胱付き腎原基にネフロン前駆細胞を注入
③ ネフロン前駆細胞を注入した膀胱付き腎原基を患者さんに移植し、臓器初期発生プログラムを遂行
④ 腎原基を移植した患者さんに尿路形成術を行い、機能的腎臓を実現
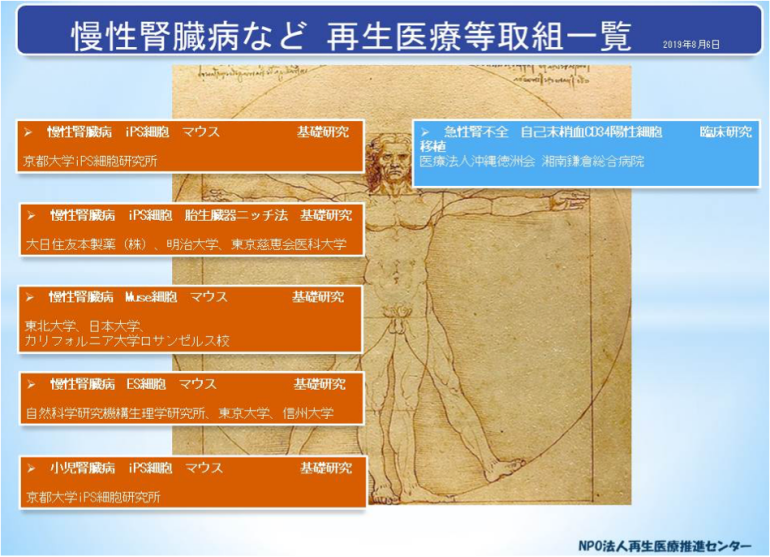
図1 慢性腎臓病などに対する再生医療等の取組状況
(用語解説)
(参考資料)
(NPO法人再生医療推進センター 守屋好文)
プライバシーポリシー
再生医療推進センターは再生医学、再生医療の実用化を通して社会への貢献を目指す非営利活動法人です。
Copyright © NPO法人再生医療推進センター All rights reserved.