
がんは日本人の死因1位の病気です。頭頸部がんは耳や鼻、口のなか、舌などにできるがんの総称ですが、がん全体の5%を占めるそうです。頭頸部がんの治療は手術、放射線、抗がん剤などで行われています。表題の治験は、免疫の働きでがん細胞を攻撃する「がん免疫療法」と呼ばれる新たな治療です。がん免疫療法はがん細胞に対する免疫反応(がん免疫)を惹起あるいは増強させ、がん免疫によりがん細胞を殺傷し、がんの進行・転移抑止、再発防止を図ります。免疫細胞の力を使ったがん免疫療法は「がん免疫細胞療法」と呼ばれます。
再生医療推進センターの再生医療トピックス No.76で「iPS細胞由来の免疫細胞でがん治療 年内にも治験へ 理化学研究所、千葉大学」で治験に向けた取組状況をご紹介しましたが、その続報です。併せまして、iPS細胞由来キラーT細胞を用いることで悪性リンパ腫の治癒に成功した取組と、遺伝子編集によるがんへの攻撃力を高めた免疫細胞をiPS細胞から作製に関する研究についてご紹介します。
千葉大学病院は、頭頸部がんの新たな治療法として、がんに対して強い攻撃力を持つ免疫細胞「NKT細胞」を用いた治療法の開発を進められてきましたが、さらなるの生存率の改善に向けて、理化学研究所と連携し、iPS細胞からNKT細胞を作製した「iPS-NKT細胞」注1)をヒトに投与する、世界初の治療法を医師主導治験として行うこと発表しました(2020年6月30日)1),2)。なお、試験名は「再発・進行頭頸部がん患者を対象としたiPS-NKT細胞動注療法に関する第1相試験」です。
同治験の目的は、今までに「iPS-NKT細胞」が人の血管内に直接投与された取組はなく、人に対する「iPS-NKT細胞」の忍容性(副作用などの発現状況を評価して適切な投与量を検討)、安全性、そして有効性について評価することにあります。その試験デザインは単施設、非盲検、非対照、用量漸増試験からなります。対象疾患は標準治療後又は標準治療の適応とならない再発・進行頭頸部がんです。対象被験者数は4~18名(副作用の発現状況による)です。なお、iPS-NKT細胞投与までの流れは次の通りです。
用いられる免疫細胞はナチュラルキラーT(NKT)細胞注2)と呼ばれ、がんを攻撃したり、ほかの免疫細胞を活性化させたりする働きがあります。ただ、人の血液中に0.01%程度しか存在しないために、実用化することは困難でした。千葉大学では、患者さん自身のNKT細胞を投与する臨床研究でも、頭頸部がんを小さくする効果を確認されています。しかし、治療に使える量まで同細胞を増やすのが難しかったそうです。また、進行がんの患者さんにはうまく機能しなかった場合もあったそうです。そのため、NKT細胞をiPS細胞にいったん戻すことで、治療に必要なNKT細胞の量と質を確保することに期待したとしています。
同治験計画では、健康な人の血液から採取したNKT細胞からiPS細胞を作製し、大量に増した後に、同iPS細胞を再びNKT細胞に変化させ、患者さんに注射します。NKT細胞をiPS細胞にすることにより、効率的にNKT細胞の量を増やすことが可能となり、細胞の質も安定しやすいとしています。
頭頸部がんは患部につながる血管から狙いやすく、作製されたNKT細胞はがん部位近くの動脈に注射されます。手術や抗がん剤などの標準的な治療の後に再発された対象被験者に対し、2年間をかけて実施されます。細胞の安全性を注視し、定期的にCTによる画像検査でがんの大きさの確認などを通して効果を確かめるとしています。
治験では、1回約5千万個の細胞(患者さんの体格によって異なる)を2週間おきに計3回注射する計画です。iPS細胞にはがん化のおそれがあるとされ、他家細胞をもとにする場合には拒絶反応に対する懸念もあります。実用化に向けては安全性の確認が欠かせません。同チームは安全性と有効性が確認されれば、将来的に肺がんなどへの応用も見据えています。頭頸部がんよりも大量の細胞の注入が必要とされ、細胞の確保や安全性など超えるべきハードルも高いですが、患者さんの数も多く、死亡率も高いがんの治療にも生かされる可能性があると期待されます。
順天堂大学医学部の安藤准教授、小松教授、東京大学医科学研究所中内特任教授らの共同研究グループは、機能的に若返ったiPS細胞由来キラーT細胞が、長期間にわたりマウス生体内で生存できることを明らかにしたと発表しました(2019年7月26日)3)。そして、末梢血由来のT細胞とは異なり、iPS細胞由来のエプスタイン・バール(EB)ウイルス注3)特異的キラーT細胞が、極めて難治性のリンパ腫であるNK細胞リンパ腫注4)の増殖を長期間にわたって強力に抑え続けることを見出し、NK細胞リンパ腫を治癒することに成功されたそうです。この成果は、難治性NK細胞リンパ腫の再発例、重症例に対するiPS細胞由来T細胞を用いた新規治療法の開発に大きく道を開く可能性があるそうです。
京都大学iPS細胞研究所と武田薬品工業(株)は、新規iPS細胞由来キメラ抗原受容体(CAR)注5)遺伝子改変T(CAR-T)細胞療法(iCART)に関する研究成果が、両社の共同研究プログラムであるT-CiRAから武田薬品に継承されたと発表しました(2019年7月16日)4)。CAR-T療法は、免疫細胞の一種であるT細胞の遺伝子を、特定のがん細胞を認識して破壊することができるように改変する、免疫療法の一種です。患者さんの血液からT細胞を抽出し、遺伝子を改変する現行の自家CAR-T療法は多くの時間と多額の費用を要します。
京都大学iPS細胞研究所の金子准教授と武田薬品株の研究者らのチームは、iPS細胞研究所において作製された「再生医療医療用iPS細胞ストック」をもとにクローン化したiPS細胞を用い、患者さんにすぐに提供可能なCAR-T療法(iCART)をT-CiRA共同研究を通じて開発しました。当該法は非臨床試験において、CD19注6)とするiCARTが強い抗腫瘍効果を発揮することが明らかにされています。今後は、iPS細胞マスターセルバンク注7)から均一な細胞製剤を大量生産する製法を開発し、現行のCAR-T療法よりも低価格で患者さんに提供することを目標としています。
新型コロナウイルス感染症が世界中で猛威を振っており、社会及び経済活動などに端倪すべからざるインパクトを与えていますが、臨床試験分野においても大きな影響を受けているようです。医療機関の負担や感染拡大への影響などを考慮し、新たな臨床試験の立ち上げや新規の患者登録が中断されており、臨床試験への新規登録患者数は大きく減少しているようです5)。新型コロナウイルス感染が収斂し、臨床試験等に悪影響を与えている障害が解消されることを切望しております。
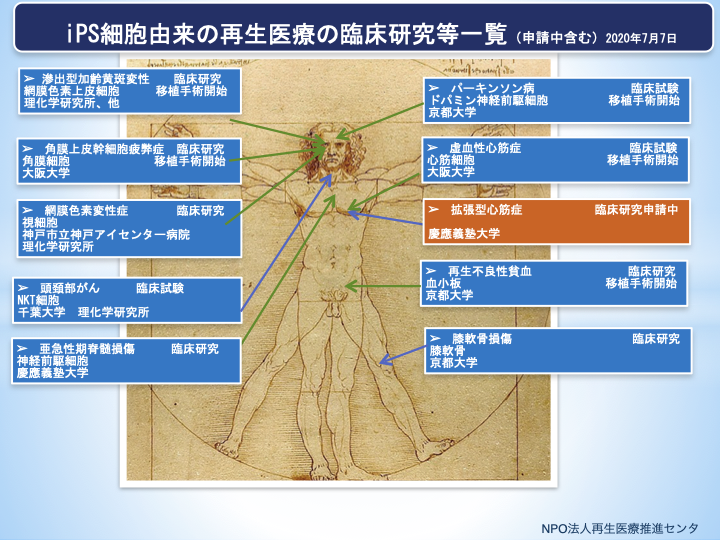
図1 iPS細胞由来の再生医療等に関する臨床研究等の取組
(y. moriya)
プライバシーポリシー
再生医療推進センターは再生医学、再生医療の実用化を通して社会への貢献を目指す非営利活動法人です。
Copyright © NPO法人再生医療推進センター All rights reserved.